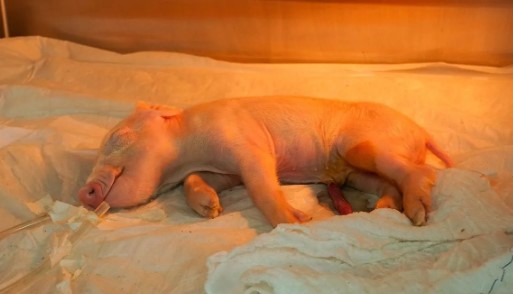
Pesquisadores vinculados ao Centro de Ciência para o Desenvolvimento em Xenotransplante (XenoBR), da Universidade de São Paulo (USP), celebraram nas últimas semanas um resultado aguardado há quase seis anos. Após diversas tentativas, o grupo conseguiu obter o primeiro porco clonado no Brasil e na América Latina.
O animal nasceu em um laboratório do Instituto de Zootecnia da Agência Paulista de Tecnologia dos Agronegócios (IZ-Apta), em Piracicaba, no interior de São Paulo. O nascimento representa um marco para o avanço de um projeto ambicioso no país: gerar suínos geneticamente modificados capazes de fornecer órgãos para transplantes em humanos sem provocar rejeição imunológica.
A iniciativa é liderada pelo cirurgião Silvano Raia, professor da Faculdade de Medicina (FM) da USP, pela geneticista Mayana Zatz, professora do Instituto de Biociências (IB) da USP e coordenadora do Centro de Estudos do Genoma Humano e Células-Tronco, um Centro de Pesquisa, Inovação e Difusão (Cepid) apoiado pela Fapesp, e pelo imunologista Jorge Kalil, professor da FM-USP.
O projeto teve início em 2019, por meio de uma parceria com a farmacêutica EMS no âmbito do Programa de Apoio à Pesquisa em Parceria para Inovação Tecnológica (Pite) da Fapesp, e ganhou escala a partir de 2022 com a criação do XenoBR, um dos centros financiados pela fundação.
“O passo que demos agora é crucial porque a clonagem de suínos é uma das técnicas mais difíceis de serem dominadas para viabilizar o xenotransplante [transferência de órgãos entre espécies diferentes]”, explica à Agência Fapesp Ernesto Goulart, professor do IB-USP e principal pesquisador do CCD.
Domínio de tecnologias
A despeito do desafio de cloná-los, os porcos têm sido escolhidos como potenciais doadores para xenotransplante por causa das semelhanças de tamanho e funcionamento de seus órgãos com os dos humanos. Além disso, são domesticados, se reproduzem bem em cativeiro e originam ninhadas grandes em poucos meses.
Se os órgãos desses animais fossem transplantados diretamente em humanos, contudo, seriam rejeitados imediatamente pelo sistema imune humano. Por isso, o genoma do animal precisa ser editado.
“O xenotransplante envolve uma cadeia de tecnologias complexas, como a modificação genética utilizando a ferramenta CRISPR/Cas9”, explica Goulart.
Com essa ferramenta, que permite inserir ou deletar nucleotídeos (blocos de construção do material genético) e até genes inteiros no genoma, os pesquisadores inativaram três genes suínos que induzem a rejeição. Com isso, utilizando técnicas de inserção gênica de precisão, que emprega uma enzima capaz de cortar a dupla fita do material genético celular em um ponto específico e inserir novos segmentos, empregaram sete genes humanos nas células suínas para torná-las mais compatíveis com o organismo do receptor.
Os embriões resultantes dessas edições foram transferidos para fêmeas híbridas (linhagens Landrace e Large White). Após uma gestação de quase quatro meses, o primeiro clone de suíno nasceu saudável, com 1,7 kg.
“O fato de o animal estar supersaudável mostra que nossa técnica funciona. Já temos outras gestações em andamento, o que reforça que dominamos o processo”, afirma o pesquisador.
Controle rigoroso e grau clínico
Os porcos clonados e as proles resultantes do cruzamento entre eles serão mantidos em dois laboratórios pioneiros de produção de suínos em grau clínico da América Latina, também construídos com apoio da Fapesp.
A instalação possui um biotério de suínos (pig facilty) com nível de biossegurança 2 (NB2) para a criação e o manejo dos porcos geneticamente modificados, livres de patógenos.
“As duas instalações têm altíssimo controle sanitário porque, no fim das contas, os órgãos que serão obtidos a partir desses animais serão um produto médico. Por isso, não pode existir o risco de transmissão de vírus, bactérias ou patógenos suínos para o receptor humano”, explica Goulart.
A expectativa dos pesquisadores é produzir inicialmente um plantel de porcos clonados composto por alguns casais. A partir desse pequeno grupo de animais, eles esperam, por meio de reprodução natural, manter e evoluir, sem a necessidade de clonar indefinidamente.
Uma das vantagens da linhagem de suínos escolhida pelos pesquisadores para obter os órgãos para xenotransplante é o crescimento rápido. Com aproximadamente 7 meses de idade, os animais já atingem o peso necessário ao transplante para um humano adulto com 80 quilos.
Tecnologia estratégica
De acordo com Goulart, teoricamente é possível aproveitar qualquer tecido ou órgão dos suínos clonados para xenotransplante. Inicialmente, porém, eles escolheram rim, córnea, coração e pele porque juntos atendem 94% da demanda do SUS, responsável pelo financiamento e pela realização de 90% a 96% dos transplantes de órgãos no Brasil.
Segundo ele, até o momento nenhum país obteve aprovação para realizar xenotransplante. A fim de viabilizar a tecnologia, estão sendo conduzidos estudos clínicos nos Estados Unidos e há outro prestes a ser iniciado na China. Com base nos resultados desses estudos será possível entender se de fato a solução funciona e qual a sobrevida média do órgão transplantado, entre outras questões.
“Mesmo se a sobrevida de um órgão transplantado for curta, ele já possibilita salvar vidas. Um paciente com hepatite fulminante tem de ser transplantado em, no máximo, uma semana. Utilizar órgãos de porco como um transplante ponte, até conseguir um transplante humano compatível, pode ser uma boa estratégia. É isso que os chineses estão fazendo”, conta Goulart.
“Os dois primeiros casos foram de transplantes cardíacos e os pacientes sobreviveram por volta de 60 dias. Também teve um transplante de rim cujo paciente sobreviveu meses e veio a falecer posteriormente em razão de um infarto não relacionado ao transplante e outro paciente em que o rim funcionou por mais de 270 dias e depois ele retornou para diálise”, pondera Goulart.
A meta dos pesquisadores é que o custo dos órgãos provenientes de porcos clonados no Brasil por meio do projeto represente uma pequena fração dos que serão comercializados pelos Estados Unidos e pela China.
CNN